— もりうち機構の反応速度定数 (Na + Cl, Na + Cl2) —
- 衝突理論 (アトキンス 27.1 章) の演習問題
演習問題
概要
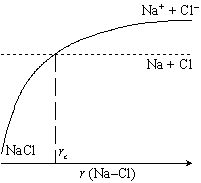
図 1-2. 「もりうち」機構
分子直径と平均並進速度のみから導かれる単純衝突理論は、
分子を硬い球であると近似したもので 「剛体球衝突理論」
と呼ばれる。 気相の化学反応は、
分子衝突が起こらなければ起こらないので、衝突速度は反応速度の
上限値であると考えることができる。
この演習で扱う 「もりうち機構」 の反応は、 ある限界距離
rc 以下に Na と Cl
が近づくと引力が働いて反応が起こる (図 1-2)、 というもので、
剛体球衝突理論の理論式で、 反応速度定数が記述される。
ただし、多くの場合は 「もりうち機構」 は定性的な説明であって、
反応速度定数の、 定量的な推定や議論に耐えるものではない。
補足説明と演習のヒント
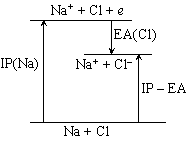
図 1-3. IP − EA
- (1-2) 式の IP − EA は Na + Cl と Na+ + Cl− のエネルギー差に相当する (反応 R1 の場合; 図 1-3 参照)。
- (1-2) 式の最後の項はクーロン引力で、ここでは SI 単位系での式を示した。 分母の 4πε0 がない式を目にすることがあるが、これは cgs-esu 単位系の式である。 SI 単位で計算する場合は、 分母の 4πε0 を忘れてはならない。
- 物理量は最も一般的に用いられる単位で示したため、
単位の換算が必要である。 以下を参照せよ。
- 1 [eV] = e [C]
 1 [V] =
e [J] = 1.6022
1 [V] =
e [J] = 1.6022  10−19 [J]
10−19 [J]
or 1 [J] = e−1 [eV] - 1 Å = 10−10 m = 10−8 cm
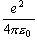 [C2
F−1 m = J m] =
[C2
F−1 m = J m] = 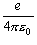 [eV m] = 14 ~ 15 [eV Å]
(下線部は自分で計算してみよ)
[eV m] = 14 ~ 15 [eV Å]
(下線部は自分で計算してみよ)
- 1 [amu] = 1 [g mol−1] = 10−3 / N A [kg (molecule−1)]
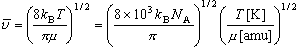
= 145 ~ 150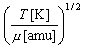 [m s−1]
(下線部は自分で計算してみよ)
[m s−1]
(下線部は自分で計算してみよ)
- 1 [eV] = e [C]
- 反応 (R2) に関しても、考え方は反応 (R1) と同様。 生成物が
NaCl2 ではなく、 NaCl + Cl となっているが、
反応速度定数は Na と Cl2
が近づくところで決定される。 (図 1-4 参照)
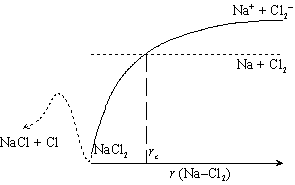
図 1-4. 反応 (R2)
- 答の値は、反応 (R1), (R2) とも以下の範囲にある。
- [問題 1-1] : rc = 1 ~ 10 Å
- [問題 1-2] :
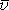 = 100 ~ 1000
m s−1
= 100 ~ 1000
m s−1
k = 10−10 ~ 10−8 cm3 molecule−1 s−1